|
МОЛЕКУЛЯРНАЯ ФИЗИКА
2.Модель идеального газа Основные предположения. 1.Число молекул в газе велико: N >> 1 , среднее расстояние между отдельными молекулами много больше их размеров (l >> a). 2.Молекулы газа совершают неупорядоченное, хаотическое движение. 3.Движение отдельных молекул подчиняется законам классической механики. При этом молекулы рассматриваются как материальные точки, совершающие только поступательное движение. Величина потенциальной энергии взаимодействия в среднем мала по сравнению со средней кинетической энергией. 4.Все соударения молекул друг с другом и со стенками сосуда, в котором находится газ, являются абсолютно упругими (происходят без потери энергии). При ударе о стенку компонента импульса молекулы, перпендикулярная стенке, меняет знак (но не величину). Таким образом, в целом выполняются законы сохранения импульса и энергии для молекул газа. Понятие об усреднении. По определению среднее значение какой-то величины, которая случайным образом в N независимых испытаниях принимает N значений a i , равно
Ввиду полной хаотичности движения молекул проекции скорости молекул на ось x с равной вероятностью могут принимать как положительные, так и отрицательные значения. Поэтому среднее значение проекции скорости i-ой молекулы на ось x равно нулю: <v ix >=0 . Аналогично <v iy >=<v iz >=0 . Однако средние значения квадратов проекций скорости не равны нулю! Определим для i-ой молекулы
Тогда
Поскольку все направления эквивалентны, то
поэтому
Основное уравнения модели идеального газа . Основное уравнение молекулярно-кинетической теории идеального газа утверждает. Произведение давления идеального газа на его объем пропорционально плотности числа молекул в газе и средней кинетической энергии поступательного движения отдельной молекулы.
|
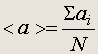
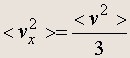
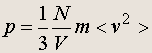
 При любом использовании материалов установите обратную ссылку на своем сайте.
При любом использовании материалов установите обратную ссылку на своем сайте.
